ဓာတ်ခွဲခန်းတွင် အသစ်တစ်ခုအနေဖြင့်၊ ပြောင်းနှုန်းနည်းသော အပင်အစုအဝေးမှ အပြုသဘောဆောင်သောအပင်များကို စစ်ဆေးရန် ကောင်းသောအလုပ်မဟုတ်ပါ။ပထမဦးစွာ DNA ကိုနမူနာအမြောက်အမြားမှတစ်ခုပြီးတစ်ခုထုတ်ယူရမည်ဖြစ်ပြီး၊ ထို့နောက်နိုင်ငံခြားမျိုးဗီဇများကို PCR မှရှာဖွေတွေ့ရှိမည်ဖြစ်သည်။သို့သော်၊ ရလဒ်များသည် ရံဖန်ရံခါတွင် ပစ္စည်းအနည်းငယ်ပါသော ကွက်လပ်များနှင့် ကြိုးဝိုင်းများ ဖြစ်လေ့ရှိသော်လည်း လွတ်သွားသော ထောက်လှမ်းမှုများ သို့မဟုတ် မှားယွင်းသော ထောက်လှမ်းမှုများ ရှိမရှိ ဆုံးဖြတ်ရန် မဖြစ်နိုင်ပေ။.ထိုသို့သော စမ်းသပ်မှု လုပ်ငန်းစဉ်နှင့် ရလဒ်များကို ရင်ဆိုင်ရန် အလွန် အကူအညီမဲ့နေပါသလား။စိတ်မပူပါနဲ့၊ ညီလေး က transgenic positive အပင်တွေကို လွယ်လွယ်ကူကူနဲ့ တိကျစွာ စစ်ဆေးနည်းကို သင်ပေးတယ်။
အဆင့် ၁
ဒီဇိုင်းထောက်လှမ်း primers
စမ်းသပ်မည့်နမူနာအရ တွေ့ရှိရမည့် endogenous gene နှင့် exogenous gene ကို ဆုံးဖြတ်ပြီး primer ဒီဇိုင်းအတွက် gene အတွက် ကိုယ်စားလှယ် 100-500bp sequence ကို ရွေးချယ်ပါ။ကောင်းသော primers များသည် ထောက်လှမ်းခြင်းရလဒ်များ၏ တိကျမှုကို သေချာစေပြီး ထောက်လှမ်းချိန်ကို တိုစေသည် (အသုံးများသော ထောက်လှမ်းရေး primers အတွက် နောက်ဆက်တွဲကို ကြည့်ပါ)။
သတိပြုရန်- အသစ်ထုတ်လုပ်ထားသော primers များသည် တုံ့ပြန်မှုအခြေအနေများကို အကောင်းဆုံးဖြစ်အောင်လုပ်ပြီး အကြီးစားရှာဖွေခြင်းမပြုမီ ထောက်လှမ်းမှု၏တိကျမှု၊ တိကျမှုနှင့် ထောက်လှမ်းမှုကန့်သတ်ချက်ကို စစ်ဆေးရန် လိုအပ်သည်။
အဆင့် ၂
စမ်းသပ်မှုပရိုတိုကောကို ဒီဇိုင်းဆွဲပါ။
အပြုသဘောဆောင်သောထိန်းချုပ်မှု- PCR တုံ့ပြန်မှုစနစ်နှင့် အခြေအနေများသည် ပုံမှန်ဟုတ်မဟုတ် ဆုံးဖြတ်ရန် ပစ်မှတ်အပိုင်းအစများပါရှိသော သန့်စင်ထားသော DNA ကို နမူနာပုံစံအဖြစ် အသုံးပြုပါ။
အနုတ်လက္ခဏာ/အလွတ် ထိန်းချုပ်မှု- PCR စနစ်တွင် ညစ်ညမ်းမှု ရင်းမြစ်ရှိမရှိ စစ်ဆေးရန် ပစ်မှတ်အပိုင်းအစများ မပါဝင်သည့် DNA နမူနာပုံစံ သို့မဟုတ် ddH2O ကို အသုံးပြုပါ။
အတွင်းအကိုးအကားထိန်းချုပ်မှု- နမူနာ၏ endogenous gene ၏ primer/probe ပေါင်းစပ်မှုကို PCR မှရှာဖွေတွေ့ရှိနိုင်သည်ရှိမရှိအကဲဖြတ်ရန် စမ်းသပ်ရန်အတွက် နမူနာကိုအသုံးပြုပါ။
အသိပေးစာ:
စမ်းသပ်မှုရလဒ်များ၏တရားဝင်မှုကိုအကဲဖြတ်ရန် စမ်းသပ်မှုတစ်ခုစီအတွက် အပြုသဘော၊ အနုတ်လက္ခဏာ/အလွတ်ထိန်းချုပ်မှုများနှင့် အတွင်းပိုင်းထိန်းချုပ်မှုထိန်းချုပ်မှုများကို သတ်မှတ်သင့်သည်။
စမ်းသပ်ပြင်ဆင်မှု
အသုံးမပြုမီ၊ ဖျော်ရည်သည် အညီအမျှရောစပ်မှုရှိမရှိ သတိပြုပါ။မိုးရွာသွန်းမှုတွေ့ရှိပါက အသုံးမပြုမီ ညွှန်ကြားချက်များအတိုင်း အရည်ဖျော်ပြီး ရောစပ်ရပါမည်။2×PCR ရောနှောခြင်းကို အသုံးမပြုမီ ပိုက်ပိုက်ဖြင့် မိုက်ခရိုပီပက်နှင့် ထပ်ခါတလဲလဲ ရောစပ်ထားရန် လိုအပ်ပါသည်။
အသိပေးစာ:
လက်စွဲစာအုပ်ကိုထုတ်ပြီး ဂရုတစိုက်ဖတ်ပါ၊ လက်စွဲ၏လိုအပ်ချက်များနှင့်အညီ တိကျသောစမ်းသပ်မှုမတိုင်မီ ကြိုတင်ပြင်ဆင်မှုများပြုလုပ်ပါ။
အဆင့် ၄
PCR တုံ့ပြန်မှုစနစ်ပြင်ဆင်ပါ။
စမ်းသပ်မှုပရိုတိုကောအရ၊ primers၊ H2O၊ နှင့် 2×PCR တို့ကို အညီအမျှ ရောစပ်ပြီး centrifuge လုပ်ပြီး တုံ့ပြန်မှုပြွန်တစ်ခုစီသို့ ဖြန့်ဝေပါ။
အသိပေးစာ:
အကြီးစား သို့မဟုတ် ရေရှည်စမ်းသပ်ခြင်းအတွက်၊ PCR ထုတ်ကုန်များကြောင့်ဖြစ်ပေါ်လာသော aerosol ညစ်ညမ်းမှုကို ထိထိရောက်ရောက်ရှောင်ရှားနိုင်သည့် UNG အင်ဇိုင်းပါဝင်သော PCR တုံ့ပြန်မှုစနစ်ကို အသုံးပြုရန် အကြံပြုထားသည်။
အဆင့် ၅
တုံ့ပြန်မှုပုံစံကို ထည့်ပါ။
Direct PCR နည်းပညာကို အသုံးပြု၍ ပြင်းထန်သော နျူကလိစ်အက်ဆစ် သန့်စင်ခြင်းလုပ်ငန်းစဉ်အတွက် မလိုအပ်ဘဲ၊ နမူနာပုံစံပုံစံကို 10 မိနစ်အတွင်း ပြင်ဆင်နိုင်ပြီး သက်ဆိုင်ရာ PCR တုံ့ပြန်မှုစနစ်ကို ထည့်သွင်းနိုင်သည်။
အသိပေးစာ:
ခွဲထုတ်ခြင်းနည်းလမ်းသည် ပိုမိုကောင်းမွန်သော ထောက်လှမ်းမှုအကျိုးသက်ရောက်မှုရှိပြီး ရရှိသောထုတ်ကုန်ကို ထောက်လှမ်းတုံ့ပြန်မှုများစွာအတွက် အသုံးပြုနိုင်သည်။
5.1- အရွက်များကို တိုက်ရိုက်ချဲ့ခြင်း။
လက်စွဲစာအုပ်ပါ ပုံ၏အရွယ်အစားအရ အချင်း ၂-၃ မီလီမီတာရှိသော အရွက်တစ်ရှူးကို ဖြတ်ပြီး PCR တုံ့ပြန်မှုစနစ်တွင် ထားရှိပါ။
မှတ်ချက်- အရွက်အပိုင်းအစများကို PCR တုံ့ပြန်မှုဖြေရှင်းချက်တွင် လုံးဝနှစ်မြှုပ်ထားကြောင်း သေချာစေပြီး အရွက်တစ်ရှူးများကို အလွန်အကျွံမထည့်ပါနှင့်။
5.2- အရွက်ခွဲနည်း
အချင်း ၅-၇ မီလီမီတာ အချင်းရှိသော အရွက်တစ်ရှူးကို ဖြတ်ပြီး အာရုံခံပြွန်ထဲတွင် ထည့်ပါ။ရင့်ကျက်သောအရွက်ကို ရွေးချယ်ပါက အရွက်၏ပင်မသွေးကြောတစ်ရှူးများကို ရှောင်ကြဉ်ပါ။Pipette 50ul Buffer P1 lysate ကို lysate သည် အရွက်တစ်ရှူးများကို လုံးလုံးလျားလျား နှစ်မြှုပ်နိုင်စေရန် သေချာစေရန်၊ ၎င်းကို အပူစက်ဘီး သို့မဟုတ် သတ္တုရေချိုးခန်းထဲတွင် ထားကာ 95°C တွင် lyse ကို 5-10 မိနစ်ကြာ ထားလိုက်ပါ။
50ul Buffer P2 neutralization ဖြေရှင်းချက်ကို ထည့်ပြီး ကောင်းစွာရောမွှေပါ။ရရှိလာသော lysate ကို ပုံစံပလိတ်တစ်ခုအဖြစ် အသုံးပြုနိုင်ပြီး PCR တုံ့ပြန်မှုစနစ်တွင် ထည့်သွင်းနိုင်သည်။
မှတ်ချက်- ပုံစံပလိတ်ပမာဏသည် PCR စနစ်၏ 5-10% အကြားဖြစ်ပြီး 20% ထက်မပိုသင့်ပါ။ (ဥပမာ၊ 20μl PCR စနစ်တွင်၊ 1-2μl ၏ lysis solution ကို 4μl ထက်မပိုစေရ)။
အဆင့် ၆
PCR တုံ့ပြန်မှု
PCR တုံ့ပြန်မှုပြွန်ကို ဗဟိုပြု၍ ချဲ့ထွင်ရန်အတွက် PCR ကိရိယာတစ်ခုတွင် ထည့်သွင်းထားသည်။
အသိပေးစာ:
တုံ့ပြန်မှုသည် အသံချဲ့စက်အတွက် သန့်စင်ခြင်းမရှိသော ပုံစံပလိတ်ကို အသုံးပြုသည်၊ ထို့ကြောင့် ချဲ့ထွင်ခြင်းစက်ဝန်းအရေအတွက်သည် သန့်စင်ထားသော DNA ပုံစံပလိတ်ကို အသုံးပြုသည့်အချိန်ထက် 5-10 လည်ပတ်မှုပိုများသည်။
အဆင့် ၇
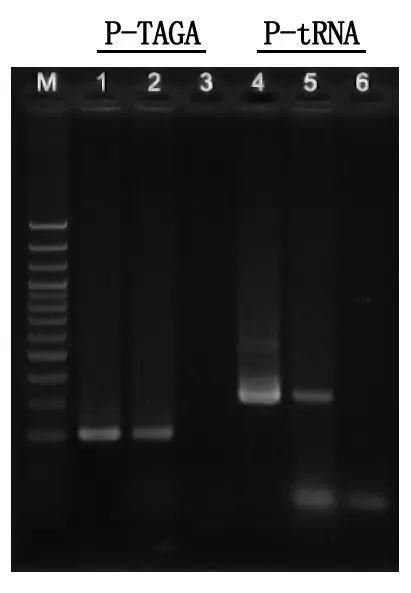
Electrophoresis ထောက်လှမ်းခြင်းနှင့် ရလဒ်ခွဲခြမ်းစိတ်ဖြာခြင်း။
M- 100bp DNA လှေခါး
1\4- သန့်စင်ထားသော DNA နည်းလမ်း
2\5- တိုက်ရိုက် PCR နည်းလမ်း
3\6- အလွတ်ထိန်းချုပ်မှု
QC-
စမ်းသပ်မှုတွင် သတ်မှတ်ထားသော ထိန်းချုပ်မှုအမျိုးမျိုး၏ စမ်းသပ်မှုရလဒ်များသည် အောက်ပါအခြေအနေများနှင့် ကိုက်ညီသင့်ပါသည်။မဟုတ်ပါက ပြဿနာ၏ အကြောင်းရင်းကို ခွဲခြမ်းစိတ်ဖြာသင့်ပြီး ပြဿနာကို ဖယ်ရှားပြီးနောက် စမ်းသပ်မှုကို ထပ်မံပြုလုပ်သင့်သည်။
ဇယား 1။ ထိန်းချုပ်မှုအုပ်စုအမျိုးမျိုး၏ ပုံမှန်စမ်းသပ်မှုရလဒ်များ
* ပလတ်စမစ်ကို အပြုသဘောဆောင်သောထိန်းချုပ်မှုအဖြစ်အသုံးပြုသောအခါ၊ endogenous မျိုးဗီဇစမ်းသပ်မှုရလဒ်သည်အနုတ်လက္ခဏာဖြစ်နိုင်သည်။
ရလဒ် စီရင်ချက်
A. နမူနာ၏ endogenous gene ၏ စမ်းသပ်မှုရလဒ်သည် အနုတ်လက္ခဏာဖြစ်ပြီး၊ သာမန် PCR ထောက်လှမ်းခြင်းအတွက် သင့်လျော်သော DNA ကို နမူနာမှ ထုတ်ယူ၍မရပါ သို့မဟုတ် ထုတ်ယူလိုက်သော DNA တွင် PCR တုံ့ပြန်မှုတားဆေးများပါရှိပြီး DNA ကို ထပ်မံထုတ်ယူသင့်သည်ဟု ညွှန်ပြပါသည်။
B. နမူနာ၏ endogenous gene ၏ စမ်းသပ်မှုရလဒ်သည် အပြုသဘောဖြစ်ပြီး၊ exogenous gene ၏ စမ်းသပ်မှုရလဒ်သည် အနုတ်လက္ခဏာဖြစ်ပြီး၊ သာမန် PCR ထောက်လှမ်းမှုအတွက် သင့်လျော်သော DNA ကို နမူနာမှ ထုတ်ယူပြီး နမူနာတွင် XXX ဗီဇကို စစ်ဆေးတွေ့ရှိခြင်းမရှိကြောင်း ဆုံးဖြတ်နိုင်သည်။
C. နမူနာ၏ endogenous gene ၏ စမ်းသပ်မှုရလဒ်သည် positive ဖြစ်ပြီး၊ exogenous gene ၏ စမ်းသပ်မှုရလဒ်သည် positive ဖြစ်ပြီး၊ သာမန် PCR ထောက်လှမ်းရန်အတွက် သင့်လျော်သော DNA ကို နမူနာမှ ထုတ်ယူထားပြီး၊ နမူနာ DNA တွင် XXX gene ပါရှိသည်။အတည်ပြုစမ်းသပ်မှုများကို ဆက်လက်လုပ်ဆောင်နိုင်သည်။
အဆင့် ၈
ဒီဇိုင်းထောက်လှမ်း primers
စမ်းသပ်ပြီးနောက်၊ ပတ်ဝန်းကျင်ညစ်ညမ်းမှုကို ကာကွယ်ရန် စမ်းသပ်ဧရိယာကို သုတ်ရန် 2% sodium hypochlorite နှင့် 70% Ethanol solution ကို အသုံးပြုပါ။
တင်ချိန်- စက်တင်ဘာ-၀၈-၂၀၂၁